Teriparatid Injekcija 20 mgje rekombinantni analog humanega obščitničnega hormona (PTH 1-34), njegova učinkovina pa ima enako zaporedje kot 34. N-terminalna aminokislina (bioaktivna regija) 84-aminokislinskega humanega obščitničnega hormona. To zdravilo spodbuja tvorbo kosti in zmanjšuje resorpcijo kosti s posnemanjem delovanja endogenega paratiroidnega hormona, s čimer poveča gostoto kosti in zmanjša tveganje za zlome. Običajne specifikacije, ki so trenutno na voljo na trgu, so 20 ug:80 ul, 2,4 ml na vialo, kar pomeni, da vsaka injekcija vsebuje 20 ug teriparatida.
V kliničnem preskušanju teriparatida je 82,8 % oziroma 84,5 % bolnikov v skupini, ki je prejemala placebo, poročalo o vsaj enem neželenem učinku. Najpogosteje poročani neželeni učinki pri bolnikih, zdravljenih s tem izdelkom, so slabost, bolečine v okončinah, glavobol in omotica. Poleg tega palpitacije, povečanje telesne mase, anemija, išias, težko dihanje, bruhanje, hemoroidi, urinska inkontinenca, poliurija, povečano znojenje, boleči mišični krči, bolečine v sklepih, krči/bolečine v hrbtu, hiperholesterolemija, zvišane ravni kalcija v krvi, hipotenzija, utrujenost, bolečine v prsih, šibkost, reakcije na mestu injiciranja (kot so bolečina, oteklina, eritem, lokalne odrgnine, srbenje in blagost) se lahko pojavijo tudi mikrokrvavitve itd.
|
|
|
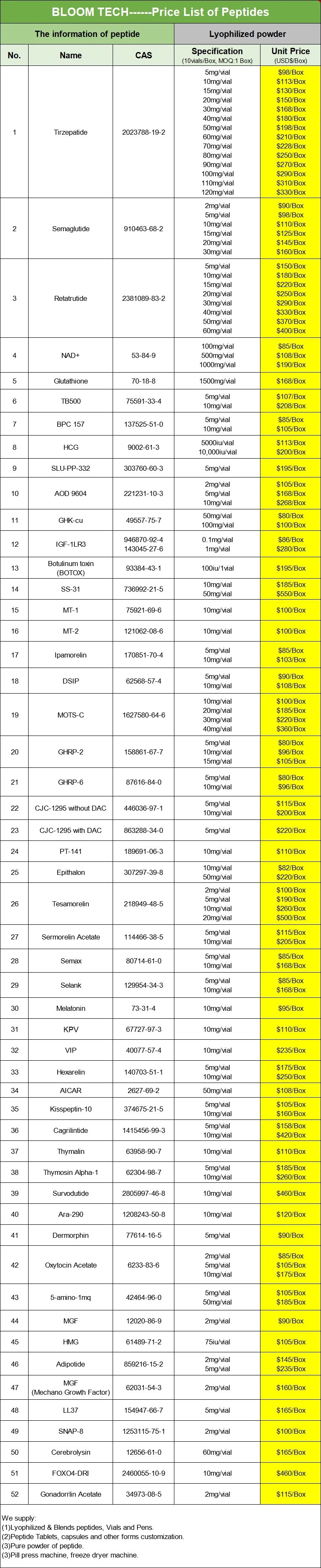



Teriparatid Powder COA



Osnovne informacije o zdravilu
Injekcija teriparatida20 mgje rekombinantni analog človeškega obščitničnega hormona (PTH 1-34), njegovo aminokislinsko zaporedje pa ima enako zaporedje kot 34. N-terminalna aminokislina (bioaktivna regija) 84-aminokislinskega človeškega obščitničnega hormona. To zdravilo je najprej razvilo podjetje Eli Lilly Nederland BV in je bilo odobreno za trženje v Združenih državah novembra 2002. To je prvo zdravilo za spodbujanje tvorbe kosti na svetu, ki se trži. Njegov izvirni raziskovalni izdelek je bil odobren za trženje na Kitajskem marca 2011, s trgovskim imenom Forsteo® /Forsteo®, specifikacija pa je 20ug:80ul, 2,4ml na vialo.
Proizvodni proces
Izrazni sistem
Injekcija teriparatida je bila pripravljena z uporabo ekspresijskega sistema Escherichia coli. Ekspresijski sistem bakterije Escherichia coli ima prednosti jasnega genetskega ozadja, enostavnega delovanja kulture, visoke učinkovitosti transformacije in transdukcije, hitre rasti in razmnoževanja ter nizkih stroškov in lahko učinkovito izraža rekombinantni človeški paratiroidni hormon (1-34).
Potek proizvodnega procesa
Konstrukcija seva in fermentacija
Vnesite gen, ki kodira teriparatid, v bakterijo Escherichia coli, da ustvarite spremenjeni sev. Nato je bil proizvedeni sev izpostavljen fermentacijski kulturi, da bi lahko izražal teriparatid v velikih količinah.
Ločevanje in čiščenje
Z nizom korakov ločevanja in čiščenja, kot so centrifugiranje, filtracija, kromatografija itd., se teriparatid loči od fermentacijske brozge, nečistoče pa se odstranijo, da se pridobi teriparatid visoke-čistosti.
Priprava
Očiščen teriparatid zmešajte s pomožnimi snovmi (kot so ledocetna kislina, natrijev acetat (brezvodni), manitol, m-krezol, klorovodikova kislina, natrijev hidroksid, voda za injekcije itd.), da pripravite raztopino za injiciranje. Med pripravo formulacije je treba parametre, kot sta pH vrednost in osmotski tlak, strogo nadzorovati, da zagotovimo stabilnost in varnost zdravila.
Polnjenje in pakiranje
Pripravljena raztopina za injiciranje se napolni v vnaprej-napolnjene injekcijske peresnike in nato zapakira. Uporaba pred-napolnjenih injekcijskih peresnikov olajša-pacientovo samoinjiciranje in izboljša njihovo skladnost.
Kontrola kakovosti
Kontrola kakovosti farmacevtskih učinkovin
Na surovini teriparatida se izvaja strog nadzor kakovosti, vključno z odkrivanjem njegove čistosti, molekulske mase, zaporedja aminokislin, biološke aktivnosti in drugih indikatorjev. Pri izdelavi pripravkov se lahko uporabljajo samo farmacevtske učinkovine, ki ustrezajo standardom kakovosti.

Kontrola kakovosti pripravkov
Izveden je celovit nadzor kakovosti injekcije teriparatida, vključno s testi videza, pH vrednosti, osmotskega tlaka, vsebine, sorodnih snovi, bakterijskega endotoksina, sterilnosti in drugih postavk. Zagotovite, da vsaka injekcija ustreza standardom kakovosti, da zagotovite varnost zdravil za bolnike.

Študija stabilnosti
Študija stabilnosti injekcije teriparatida je bila izvedena, da bi raziskali njegovo stabilnost v različnih pogojih, kot sta temperatura in vlažnost. Na podlagi rezultatov študije stabilnosti določite rok uporabnosti in pogoje shranjevanja zdravila.

Raziskave in razvoj ter lansiranje generičnih zdravil na trg
Napredek raziskav in razvoja
Trenutno so številna domača podjetja izvedla raziskave in razvoj generičnega injiciranja teriparatida. Na primer, injekcija teriparatida podjetja Xinlitai (Suzhou) Pharmaceutical je bila aprila 2022 uspešno odobrena za trženje in je postala prva domača injekcija teriparatida, ki je bila odobrena. Poleg tega je več podjetij predložilo vloge za trženje za ta projekt v kategoriji terapevtskih bioloških proizvodov razreda 3.3 ali kemičnih zdravil razreda 4.
Bioekvivalenčne študije
Za raziskave in razvoj generičnih zdravil je treba izvesti bioekvivalenčne študije, da se dokaže, da med generičnimi zdravili in originalnimi zdravili ni klinično pomembnih razlik v varnosti in učinkovitosti. Za polipeptidni produkt z majhno molekulo rekombinantnega izvora, kot je injekcija teriparatida, ki ima preprosto strukturo in nizko tveganje imunogenosti, če se natančnejša farmacevtska analiza in karakterizacija izkažeta za podobne izvirnemu raziskovalnemu izdelku, lahko študija enakovrednosti farmakokinetike z referenčnim zdravilom podpre njegovo trženje kot biološko podobno zdravilo.
Objav{0}}nadzor kotacije
Po uvedbi generičnih zdravil na trg je treba okrepiti nadzor, da bosta njihova kakovost in učinkovitost skladni s kakovostjo in učinkovitostjo originalnih raziskovalnih zdravil. Regulativni organi za zdravila bodo izvajali redne naključne preglede generičnih zdravil in resno obravnavali izdelke, ki ne izpolnjujejo standardov kakovosti.
Skladiščenje in transport
Injekcija teriparatida20 mgshranjujte v hladilniku pri 2 do 8 stopinjah, pri čemer se izogibajte zmrzovanju. Med transportom je treba vzdrževati tudi ustrezne temperaturne pogoje, da zagotovimo kakovost in stabilnost zdravil. Po vsakem injiciranju mora bolnik ta izdelek shraniti v hladilniku. Če je raztopina motna, obarvana ali vsebuje delce, je ne smete uporabiti.
Varnost in toleranca
Pogosti neželeni učinki




Reakcija na mestu injiciranja
Bolnik lahko na mestu injiciranja občuti rdečico, oteklino, bolečino ali srbenje. Te reakcije so običajno blage in v večini primerov ne zahtevajo posebnega zdravljenja. S podaljševanjem časa zdravljenja lahko simptomi postopoma izzvenijo.
Sistemski neželeni učinki
Slabost, glavobol in omotica: To so razmeroma pogosti sistemski neželeni učinki, ki so običajno blagi in jih večina bolnikov dobro prenaša.
Bolečina v okončinah: nekateri bolniki lahko občutijo bolečino v okončinah, ki je lahko povezana s spremembami v presnovi kosti med procesom tvorbe kosti, ki ga spodbujajo zdravila.
Krči v nogah: Pri majhnem številu bolnikov se lahko pojavijo krči v nogah, kar ima lahko določen vpliv na njihovo vsakdanje življenje.
Hiperkalciemija
Prekomerna vsebnost kalcija v krvi je manifestacija hiperkalcemije. Teriparatid lahko spodbudi sproščanje kostnega kalcija v kri, kar povzroči prehodno povečanje koncentracije kalcija v krvi. V kliničnih preskušanjih je incidenca hiperkalciemije približno 11 % in je pogostejša pri bolnikih s kronično ledvično boleznijo v stadiju 3-4, zlasti pri tistih, ki uporabljajo dodatke kalcija v kombinaciji z dnevnim odmerkom nad 1000 mg. Pristop zdravljenja je bil prekinitev dajanja, dokler se raven kalcija v krvi ne doseže<2.6mmol/L, and then reduce the dosage to 10μg/ day.
Drugi redki neželeni učinki
Vključno s prehodno ortostatsko hipotenzijo, krči, bolečinami v sklepih, bolečimi trebušnimi krči, nagonom po defekaciji, drisko itd. V zelo redkih primerih se lahko pri bolnikih pojavijo resni neželeni učinki, kot so visoka vročina, mrzlica in hudi izpuščaji.
Varnost posebnih skupin

Bolniki z ledvično insuficienco
Bolniki s hudo ledvično insuficienco:Teriparatid injekcija 20 mgje kontraindiciran. Ker sta presnova in izločanje zdravil v telesu lahko prizadeta, kar povzroči kopičenje zdravil v telesu in poveča tveganje za neželene učinke.
Bolniki z zmerno ledvično insuficienco: Ta izdelek je treba uporabljati previdno. Med uporabo je treba skrbno spremljati delovanje ledvic in koncentracijo kalcija v krvi ter na podlagi rezultatov spremljanja prilagoditi načrt zdravljenja.
Bolniki z okvarjenim delovanjem jeter
Trenutno ni bilo opravljenih ustreznih raziskav pri bolnikih z motnjami delovanja jeter. Uporabljati ga je treba previdno pod vodstvom zdravnika. Ker imajo jetra pomembno vlogo pri presnovi zdravil, lahko jetrna disfunkcija vpliva na presnovne procese zdravil, s čimer vpliva na varnost in učinkovitost zdravil.


Otroci in mladostniki z odprtimi epifizami
Izkušenj z uporabo pri otrocih in mladostnikih, mlajših od 18 let, ni, prav tako se ne sme uporabljati pri otrocih in mladostnikih, mlajših od 18 let, in mladostnikih z odprtimi epifizami. Razvoj kosti pri otrocih in mladostnikih še ni zrel. Učinek teriparatida na njihov razvoj kosti ni jasen in njegova uporaba ima lahko škodljive učinke na rast kosti.
Starejši bolniki
Odmerka ni treba prilagajati glede na starost. Vendar imajo lahko starejši bolniki več kroničnih bolezni, njihove fizične funkcije se lahko zmanjšajo in njihova toleranca za zdravila je lahko slaba. Med postopkom zdravljenja je treba pozorno spremljati pojav neželenih učinkov.

Dolgotrajna-varnost
Tveganje za osteosarkom
Poskusi na živalih so pokazali, da dolgoročno injiciranje -visokih-odmerkov (več kot ali enako 60 ug/kg/dan) teriparatida predstavlja tveganje za osteosarkom. Vendar pa v poskusih na ljudeh po 20-letnem spremljanju doslej niso ugotovili povečanja tveganja. Kljub temu je pri uporabi teriparatida še vedno potrebna previdnost, zlasti pri bolnikih z družinsko anamnezo kostnih tumorjev ali drugih možnih dejavnikov tveganja.
Kardiovaskularna varnost
V večini kliničnih študij teriparatid ni bil pomembno povezan s srčno-žilnimi dogodki. Vendar pa so nekatere študije poročale, da se lahko pri bolnikih po uporabi teriparatida za kratek čas poveča srčni utrip. Zato je pri bolnikih z anamnezo bolezni srca in ožilja potrebna velika previdnost pri uporabi. Zdravniki morajo oblikovati ustrezne načrte zdravljenja glede na individualna stanja bolnikov ter oceniti in obvladati možne dejavnike tveganja.
Varnost medsebojnega delovanja zdravil

Medsebojno vpliva na učinkovitost dihidroklorotiazida
Opravljene so bile ustrezne študije in niso odkrili klinično pomembnih interakcij. To pomeni, da pri uporabi teriparatida v kombinaciji z dihidroklorotiazidom ni treba prilagajati odmerka zdravila, vendar je treba bolnikov odziv še vedno natančno spremljati.
Uporablja se v kombinaciji z raloksifenom ali hormonsko nadomestno terapijo
Ne spremeni učinka teriparatida na kalcij v krvi ali urinu, niti ne spremeni njegovih kliničnih neželenih učinkov. To zagotavlja določeno raven varnosti za bolnike, ki morajo ta zdravila uporabljati v kombinaciji, vendar morajo še vedno upoštevati zdravnikov nasvet, ko jih uporabljajo v kombinaciji.

Nadzor in upravljanje varnosti
Ker lahko teriparatid povzroči zvišanje koncentracije kalcija v krvi, je treba med zdravljenjem redno spremljati ravni kalcija in fosforja v krvi. Če se pri spremljanju kalcija v krvi zbirajo vzorci krvi za spremljanje kalcija v krvi, je treba to opraviti med 4 in 6 urami po zadnjem injiciranju tega zdravila, saj koncentracija kalcija v krvi takrat doseže svoj vrh, kar lahko natančneje odraža učinek zdravila na kalcij v krvi.
Med obdobjem zdravljenja morajo biti bolniki zelo pozorni na svoje telesne reakcije in zdravniku sporočiti morebitna nenormalna stanja. Zdravniki se morajo glede na resnost neželenih učinkov odločiti, ali naj prilagodijo odmerek zdravila ali prekinejo zdravljenje. Pri resnih neželenih učinkih je treba pravočasno sprejeti ustrezne ukrepe zdravljenja.
Zdravniki morajo oblikovati ustrezne načrte zdravljenja glede na individualna stanja bolnikov, kot so starost, spol, anamneza in sočasno jemanje zdravil, ter oceniti in obvladovati možne dejavnike tveganja. Med postopkom zdravljenja je treba načrt zdravljenja pravočasno prilagoditi na podlagi bolnikovega odziva in rezultatov spremljanja, da se zagotovi varnost bolnika.
Priljubljena oznake: teriparatid injekcija 20 mg, dobavitelji, proizvajalci, tovarna, veleprodaja, nakup, cena, razsuto, za prodajo